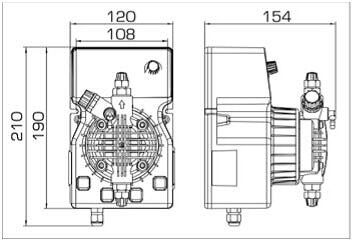
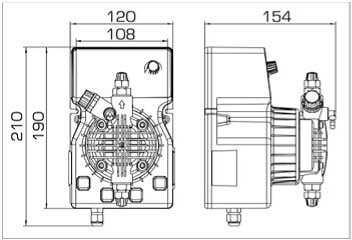
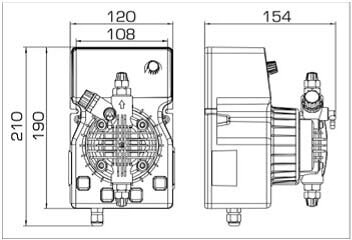
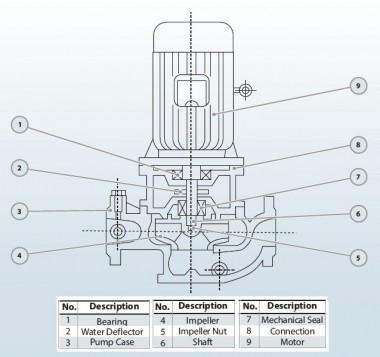
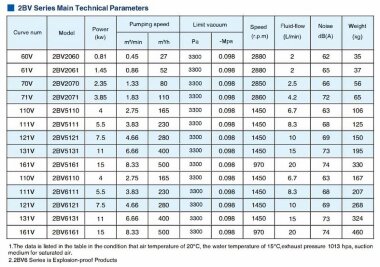
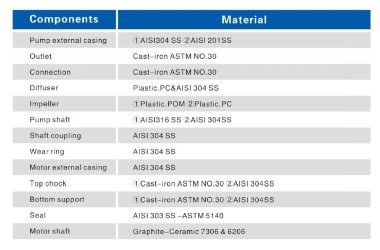
Installation automatique pour le contrôle et le dosage de l'hypochlorite de sodium
Système technologique

Actuellement, la désinfection de l'eau potable de l'entreprise est effectuée à l'aide de chlore gazeux dans des unités de chloration de type éjection. Le chlore est fourni par un système de canalisations de chlore vers des réservoirs d'eau propre, où le chlore gazeux entre en contact avec l'eau potable.
En raison du fait que le chlore est une substance très toxique et que le transport et le stockage du chlore gazeux sont explosifs, son utilisation constitue une menace pour le personnel de service et la population vivant à proximité des stations de pompage, il est donc recommandé de passer à des méthodes alternatives d'eau désinfection (ultraviolets, hypochlorite de sodium, ozonation, etc.). Parmi les méthodes de désinfection de l'eau répertoriées, seules les substances contenant du chlore ont un effet secondaire désinfectant pendant une certaine période de temps. Par conséquent, le moyen le plus pratique et le plus rentable de désinfecter l'eau potable consiste à utiliser une solution d'hypochlorite de sodium (NaClO).
Caractéristiques de l'hypochlorite de sodium
La méthode la plus fiable et la plus rentable de désinfection de l'eau potable est sa chloration, et l'hypochlorite de sodium fait référence à des réactifs contenant du chlore, qui se caractérisent par la capacité de conserver l'effet désinfectant pendant une longue période lors du transport de l'eau à travers des tuyaux, mais au en même temps, il est moins toxique que le chlore liquide. L'hypochlorite de sodium est le moins toxique et rare, relativement bon marché par rapport aux autres réactifs contenant du chlore actif.
Une solution d'hypochlorite de sodium NaCLO est obtenue par électrolyse du sel commun. Les plus stables sont les solutions d'hypochlorite de sodium à pH >11. Avec les hydrates d'hypochlorite de sodium, le plus stable est le NaCLO · 5H2O hydraté. Les facteurs qui affectent considérablement la stabilité des solutions d'hypochlorite de sodium comprennent la concentration et la température.
Ainsi les solutions contenant 250 g/l de NaCLO perdent à température ambiante la moitié du chlore actif en 5 mois, 100 g/l de NaCLO - en 7 mois, 50 g/l - en 2 ans, 25 g/l en 5...6 ans. A une température de 60°C, une solution contenant 50 g/l de NaCLO perd la moitié du chlore actif en 13 jours, et à 100°C - en 5h00.
Lorsqu'il est exposé à la lumière, le taux de programme NaCLO augmente d'environ un facteur de deux. Pour améliorer la stabilité, les solutions de NaCLO sont stockées dans l'obscurité à basse température. Si une certaine quantité de MgSO4 est ajoutée à une solution d'hypochlorite de sodium, l'hydroxyde de magnésium précipite, ce qui capture les ions de métaux lourds, augmentant la stabilité de l'hypochlorite. On sait que la stabilité de l'hypochlorite de sodium augmente en présence de silicate de sodium dans le rapport molaire
Na2O: SiO2 1:1 à 1:2 ... 1:3,5
L'effet stabilisant sur les solutions d'hypochlorite de sodium est réalisé par la gélatine, la caséine ou leur mélange. Par exemple, une solution de NaOH à 8% est chlorée à pH 8,4 ... 8,6, puis 0,3% de gélatine est ajoutée et pH=9,2 ... 9,4 est réglé. Une solution stable contenant 7,5 ... 8,0 % de NaCLO est obtenue. L'hypochlorite de sodium est produit sous forme de solutions contenant environ 15 % de chlore actif. Pour les particuliers, ces solutions sont diluées à 5 et 10 %.
- Propriétés chimiques et physiques :
- formule chimique - NaClO;
- état d'agrégation: solution aqueuse. La forme solide n'est pas stable. Au contact de l'air, le produit passe rapidement à l'état liquide;
- point d'ébullition - se décompose à des températures supérieures à 35 °C;
- densité - 1,12 g/cm3;
- solubilité dans l'eau - 82% à t=25 °C;
- pH - pH=11 ;
- apparence - liquide du jaune-vert au rouge;
- odeur - chlore fort;
- volatilité - lors de la décomposition, du chlore, de l'oxyde de sodium est libéré;
- réactivité - un agent oxydant puissant, réagit avec les métaux, provoque la corrosion des métaux.
- Risque d'incendie et d'explosion:
- explosif ininflammable. Favorise la combustion, car c'est un agent oxydant puissant (en contact avec des substances organiques combustibles - la sciure de bois, les chiffons et autres pendant le processus de séchage peuvent provoquer une combustion spontanée);
- limite de température de propagation de la flamme - ne brûle pas;
- limite de concentration de propagation de la flamme - ne brûle pas;
- la possibilité de destruction thermique, produits éducatifs - chlore, oxyde de sodium;
- agents d'extinction d'incendie - sont sélectionnés en fonction des propriétés explosives et dangereuses des matériaux combustibles situés dans la zone d'incendie avec ce produit, en tenant compte de la présence dans les hypochlorites à fort pouvoir oxydant;
- mesures spéciales de sécurité incendie - éviter de chauffer à 70 °C et plus (décomposition explosive). Stocker à l'écart des matériaux combustibles.
- Toxicité:
- cumulatif - faible;
- le tableau clinique de l'empoisonnement aigu - mal de gorge, toux, respiration irrégulière, douleurs abdominales, diarrhée, vomissements, confusion, coma, choc.
- les organes et systèmes les plus vulnérables - le système nerveux central, le système respiratoire, le foie, les reins, le pancréas, la peau, les yeux;
- doses (concentrations) qui ont un effet toxique:
- DEmin=1000 mg/kg (humain, i.v. une fois selon l'effet sur le système nerveux central);
- DEmin=45 mg/kg (individuel, intraveineux, selon l'effet sur le système nerveux central);
- action de résorption cutanée - non;
- effet sensibilisant - oui;
- action emdriotoxique - non étudiée;
- action gonadotoxique - oui;
- action mutagène - oui.
- L'effet de l'hypochlorite de sodium sur le corps humain:
- Selon le degré d'impact sur le corps humain, l'hypochlorite de sodium de grade "A" appartient aux substances de la 3ème classe de danger conformément à GOST 12.1.007-76, en tant que substance modérément dangereuse lorsqu'elle est injectée dans l'estomac et à la 4ème classe de substances à faible risque lorsqu'il est appliqué sur la peau, ce qui provoque une irritation locale modérée de la peau et s'exprime sur la muqueuse des yeux.
- L'hypochlorite de sodium à des concentrations de 0,5-0,3% (par préparation) ne provoque pas d'irritation locale sur la peau avec un seul contact, à des concentrations de 4-5% il provoque une légère irritation. En cas de contact répété, il provoque un dessèchement de la peau après 2-3 applications.
- La substance présente un danger d'inhalation en raison de la libération de chlore dans l'air, qui irrite les muqueuses des yeux et des organes respiratoires.
- La concentration maximale autorisée dans l'air de la zone de travail est de 1,0 mg/m3 (classe de danger 2 selon GOST 12.1.007-76)
- La concentration maximale admissible dans l'air atmosphérique est de 0,1 mg/m3.
Calcul de la consommation de solution d'hypochlorite de sodium
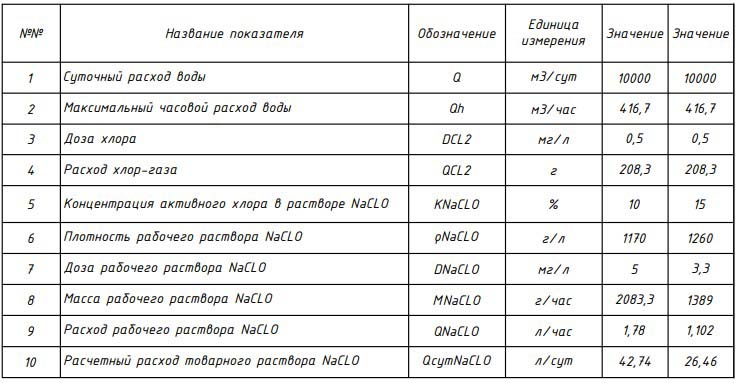
Le calcul de la consommation d'hypochlorite de sodium (NaCLO) effectué pour une solution de NaCLO à 6 % est donné sous forme de tableau.
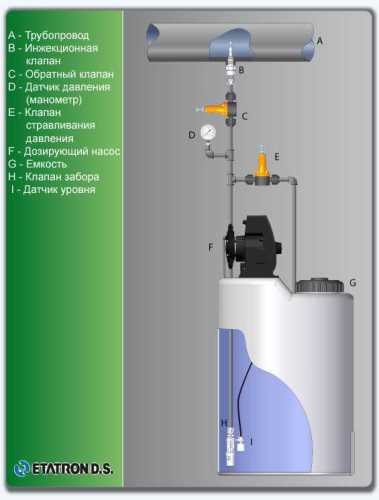
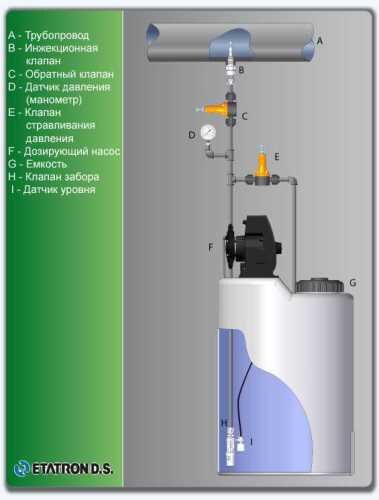
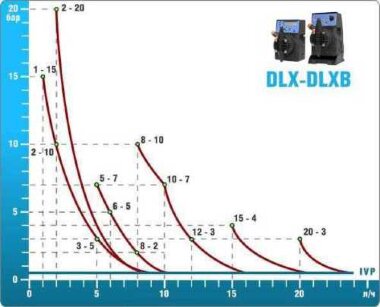
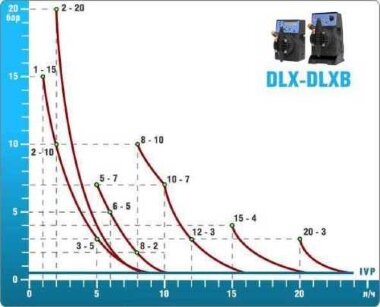
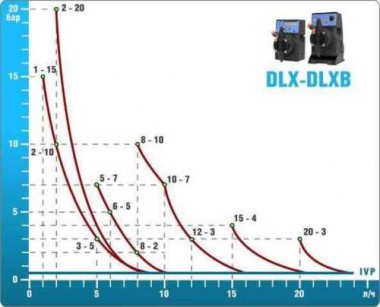
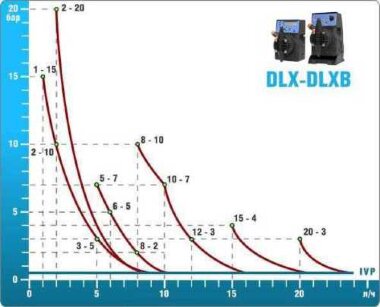
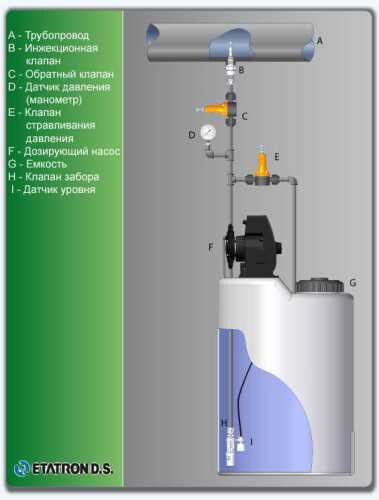
Équipement technologique
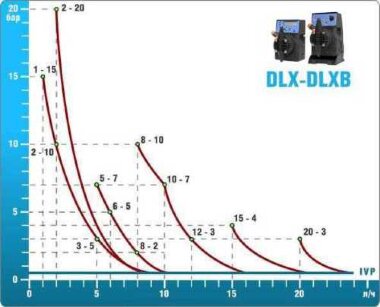
- Selon les calculs, pour le contrôle et le dosage de la solution d'hypochlorite de sodium,
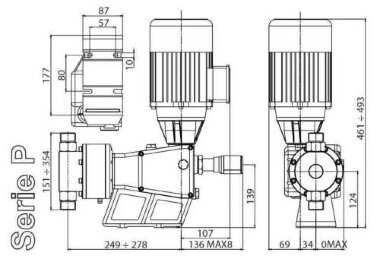
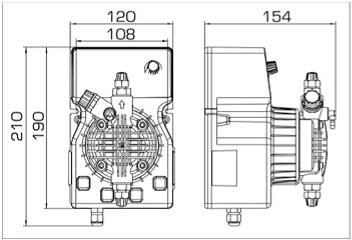
Equipement ETATRON D.S.:
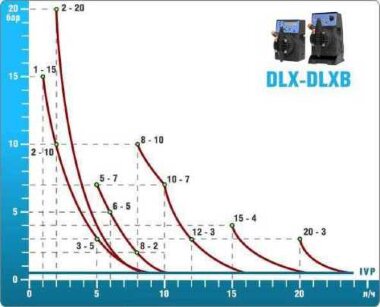
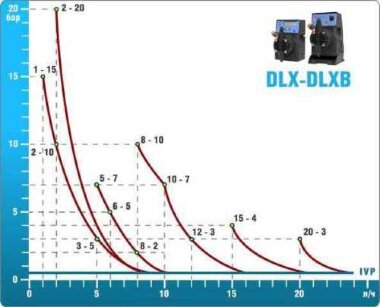
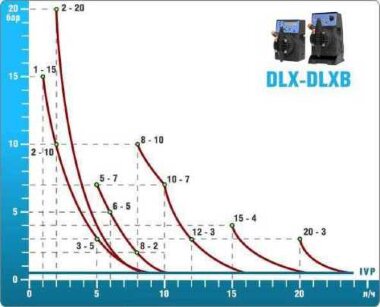
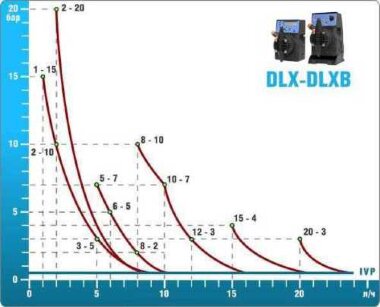
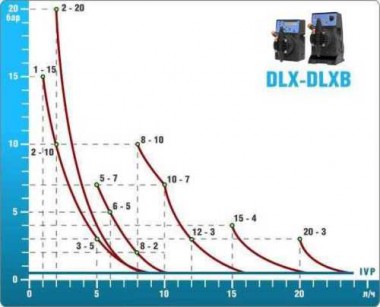
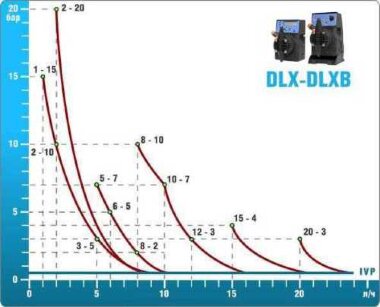
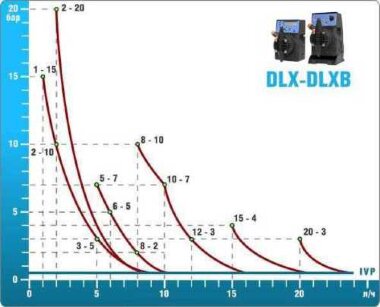
- pompes doseuses d'une capacité de 16 l/h, 14 bar
Les pompes doseuses sont contrôlées par le contrôleur de chlore Etatron eSELECT B1. - La valeur de la dose de chlore est déterminée à l'aide du capteur de chlore galvanométrique Etatron SCLO3.
En fonction de la dose de chlore réglée sur le contrôleur, une sortie relais proportionnelle de 4-20 mA est activée, qui régule le fonctionnement du convertisseur de fréquence de la pompe.
Dans ce cas, la valeur maximale du signal analogique est de 20 mA et la pompe doseuse fonctionne à sa capacité maximale. Lorsque la valeur de la dose de chlore s'approche de la valeur réglée sur le contrôleur, la valeur du signal diminue proportionnellement et, lorsque la valeur réglée est atteinte, est égale à 4 mA. Dans ce cas, le relais du contrôleur s'éteint et le convertisseur de fréquence de la pompe doseuse s'arrête à mode veille.
Calcul de la consommation d'hypochlorite de sodium (NaCLO)